
Copyright
© 2000-2015
LHERBAUDIERE

6 pages à l'impression

18 mars 2013
 |
Copyright |
 6 pages à l'impression |
 |
version initiale 2003 | |
| dernière
mise à jour 18 mars 2013 |
| un
autre domaine |
||||
la
méthode essentielle |
||||
une
variante chimique |
||||
| une collection d'icônes pour visiter tout le site | ||||
Pour identifier qualitativement et/ou quantitativement une espèce chimique dans ces types d'application deux voies principales sont suivies :généralités
Un certain nombre de travaux ont été menés dans les 20 dernières années en vue de réaliser des capteurs microchimiques en exploitant divers procédés physicochimiques. Dans tous les cas l'objectif est de disposer de microcapteurs pour les analyses essentiellement biochimiques dont les applications relèvent soit du contrôle qualité dans le domaine de l'agro-alimentaire, soit de l'analyse médicale. Domaine que l'on peut lui-même scinder en deux types d'application, celles in vivo c'est à dire directement dans le corps humain et celles relevant plus particulièrement du laboratoire de microanalyse exploitant un micro-échantillon.
soit l'espèce chimique est adsorbée physiquement sur un substrat,Quel que soit le procédé de mesure retenu on va devoir fixer le composé qui réagira physiquement ou chimiquement avec la substance à détecter sur un substrat adapté au processus de mesure choisi. Ce sont ces méthodes de fixation d'une microcouche d'un élément réactif spécifique que nous allons examiner ici.
soit elle réagit chimiquement avec l'un des composants du substrat
et pour quantifier le résultat on exploitera soit une variation de masse de l'ensemble (microbalance à quartz) soit la modification d'une propriété physique, le plus souvent par voie optique ou hyper fréquence, d'un élément du dispositif, que nous présentons par ailleurs (capteurs biochimiques)
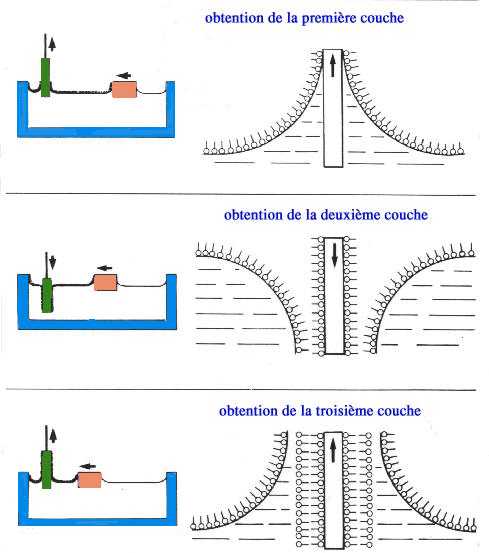
Historiquement, le physicien américain Langmuir et son assistante Miss Blodgett mirent en évidence le fait qu'une goutte d'huile (molécule amphiphile) déposée sur une surface statique d'eau, s'étale jusqu'à former un film monomoléculaire. Ce film, moyennant quelques précautions, pourra être récupéré sur une surface propre et présente des propriétés tout à fait remarquables. Cette idée a été mise en oeuvre en France par le physicien André Barraud au CEA-Saclay afin d'en faire une procédure reproductible de production de films monomoléculaires exploitables dans diverses applications allant des procédés anti-friction aux biocapteurs.
films de LANGMUIR-BLODGETT

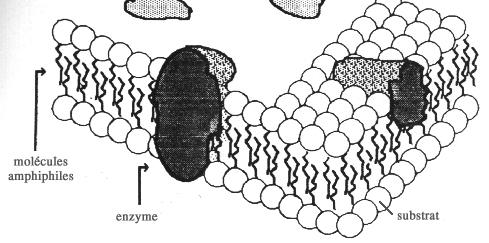
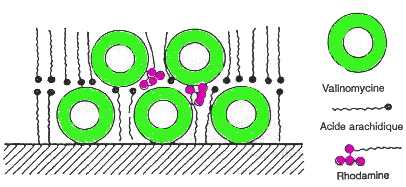
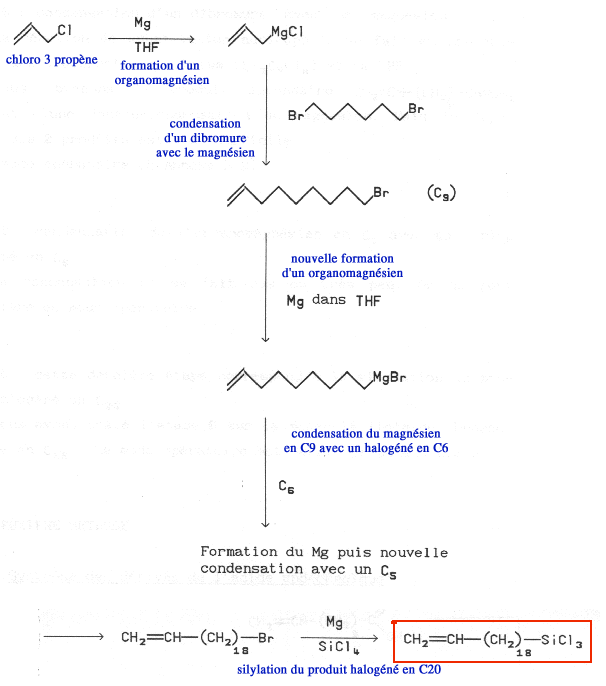
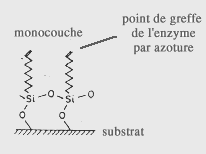
Une seconde procédure, permettant de fixer une enzyme sur une surface cette fois-ci métallique, est due à l'israélien Sagiv. Elle repose sur la formation d'une liaison chimique covalente entre le support et les molécules. Elle implique aussi l'emploi de molécules intermédiaires à longue chaîne dont l'une des extrémités comporte un groupement se fixant relativement facilement sur une surface métallique et l'autre extrémité un groupement fixant l'enzyme. La réalisation de cette procédure implique la mise en oeuvre de techniques de synthèse organique assez complexes pour générer ce type de molécules non courantes. A titre indicatif nous donnons ci-dessous la succession des opérations conduisant du chloro 3 propène, matériau commercialisé, au dérivé silané permettant la fixation de l'uréase, première enzyme mise en oeuvre dans un tel biocapteur.méthode de SAGIV
 |